ارجووو منكم ولا هنتوا
تساعدوني باوراق عمل عن التغيرات الفيزيائية والكيميائية ضروووري
الله يخليكم
ولكم جزيل الشكر والعرفان

I wanaa too
ارجووو منكم ولا هنتوا
تساعدوني باوراق عمل عن التغيرات الفيزيائية والكيميائية ضروووري
الله يخليكم
ولكم جزيل الشكر والعرفان

الرابط : –
http://mssuae.com/vb/showthread.php?t=216
|
السلام عليكم ورحمة الله وبركاته
شكرا لجهودكم الطيبة في المنتدى جعل الله كل ما تقدمونه في ميزان أعمالكم وننتظر ابداعكم القادم |
كيف تبحث في الشبكة عن الفلاشات الكيميائية ؟
1- اذهب الى موقع محرك البحث مثل :
http://www.google.com
http://www.google.com/options/universities.html (موقع يبحث في مواقع الجامعات التعليمية فقط ).
http://www.*******.overture.com/d/
موقع رائع للبجث
او اي موقع بحث اخرى .
2- ادخل كلمات البحث عن الفلاشات الكيمياء باللغة الانكليزية في مربع البحث مثل :
chem flash *********
او chem flash movie
او chem swf
او chem flash portfolio
او chem flash gallery
او flash ********* chemischer
واذا كنت تبحث في مجال معين في الكيمياء (مثل التفاعل الكيميائي او الكيماء الحرارية او الكيمياء النووية وغيرها طبعا ،تجدها في القواميس، فقم بتبديل كلمة (chem) الى الكلمة المناسبة في ذلك المجال .مثل :
الكيمياء الحيوية biochemistry
التفاعل الكيميائي reaction
نفط petroleum
لافلزي non ****llic
كيمياء نووية nuclear
كيمياء حرارية thermochemistry
كيمياء عضوية organic chemistry
كيمياء كهربائية electrochemistry
مثال : nuclear flash *********
ودمتم سالمين ….
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |
| أنواع التفاعلات الكيميائي1.pdf (446.8 كيلوبايت, المشاهدات 582) |

 ولاتنسوا الردود
ولاتنسوا الردود
وهذا ايميلي للتواصل**
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
والله حلوو ^__^
يعطيك العافيه
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
والله يعطيك العافية
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
|
مشكور اخوي على الحلول
وما تقصر |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
و يزاك الله خير …
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |

| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
يعطيكم الصحه والعافيه
| الحسابات الكيميائية للغازات.doc (128.5 كيلوبايت, المشاهدات 1443) |
ورقة عمل بسيطة لتغيرات الكيميائية و الفيزيائية
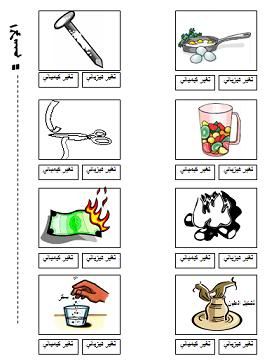
التحميل من الرابط أو من المرفقات
http://www.mediafire.com/?4d7lznzc74mmpqt
لا تنسونا من دعائكم الصالح و بالتوفيق لي بالدراسة و لوالدتي رحمها الله وغفر لها
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
للرفع ليتزامن مع وقت الدرس
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
جزاك الله خير
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
| التغيرات الفيزيائة و الكيميائية.rar (145.2 كيلوبايت, المشاهدات 336) |
|
مع أخر 6 أوراق عمل للحسابات الكيميائية ( من 22 -27 ) تتبع استراتيجية كتاب المعلم نرجو من الله أن تحقق لكم الاستفادة القصوى
ولا تنسونا من صالح الدعوات |